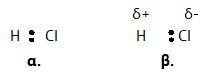Θεωρία
Έχει αναγνωσθεί 4165 φορές!
1.1 Διαμοριακές δυνάμεις
Ενδομοριακοί δεσμοί
Γιατί σχηματίζονται οι χημικοί δεσμοί
Στην Α΄ Λυκείου μάθαμε πως ο λόγος που σχηματίζονται τα μόρια των ουσιών ή οι ιοντικές ενώσεις είναι η «ανάγκη» των ατόμων να αποκτήσουν σταθερή δομή ευγενούς αερίου. “Θέλουν» δηλαδή να αποκτήσουν μία συμπληρωμένη εξωτερική στιβάδα με οκτώ ηλεκτρόνια ή δύο αν πρόκειται για τη στιβάδα Κ.
Ιοντικός δεσμός
Ο πρώτος τρόπος είναι τα άτομα να αποβάλλουν ή να προσλαμβάνουν ηλεκτρόνια και μετατρέπονται σε ιόντα και σχηματίζουν ιοντικές ενώσεις. Ο δεσμός λέγεται ιοντικός ή ετεροπολικός δεσμός και οφείλεται στις ισχυρές ηλεκτρικές ελκτικές δυνάμεις μεταξύ των ετερώνυμων ιόντων που τις αποτελούν. Τα ιόντα των ενώσεων συγκρατούνται σε διατάξεις που λέγονται κρυσταλλικά πλέγματα. Οι ιοντικές ενώσεις είναι στερεές, ενδεικτικό της μεγάλης ισχύος του ιοντικού δεσμού.
Ομοιοπολικός δεσμός
Ο δεύτερος τρόπος που τα άτομα χρησιμοποιούν για να αποκτήσουν δομή ευγενούς αερίου είναι να συνεισφέρουν ηλεκτρόνια οπότε σχηματίζονται μοριακές (=ομοιοπολικές) ουσίες μεταξύ ατόμων. Οι ομοιοπολικές ενώσεις μπορούν να είναι στερεές, υγρές ή αέριες.
Σχέση της φυσική κατάστασης των ουσιών με τις δυνάμεις μεταξύ των μορίων
Η φυσική κατάσταση των ουσιών επηρεάζεται επίσης δύο αντιμαχόμενες δυνάμεις που ασκούνται ανάμεσα στα μόρια.
Οι πρώτες, οι οποίες οφείλονται στη θερμική κίνηση των μορίων, τείνουν ν’ απομακρύνουν τα μόρια το ένα από το άλλο.
Οι δεύτερες, που είναι ηλεκτρικής φύσης, είναι ελκτικές δυνάμεις και τείνουν να φέρουν το ένα μόριο κοντά στο άλλο. Λέγονται διαμοριακές δυνάμεις.
Το αποτέλεσμα αυτής της διαμάχης και οι ισορροπίες που αναπτύσσονται καθορίζουν, τη φυσική κατάσταση του σώματος, σε κάθε δεδομένο σύνολο συνθηκών θερμοκρασίας και πίεσης.
Διαμοριακές δυνάμεις
Ανάμεσα στα μόρια ουσιών ασκούνται δυνάμεις που λέγονται διαμοριακές δυνάμεις. Οι διαμοριακές δυνάμεις είναι πολύ ασθενέστερες από τις δυνάμεις που αποτελούν το χημικό δεσμό (τον ιοντικό ή τον ομοιοπολικό δεσμό).
Οι δυνάμεις μεταξύ των μορίων των ομοιοπολικών ενώσεων λέγονται διαμοριακές δυνάμεις.
Προκειμένου να κατανοήσουμε πώς οι λειτουργούν οι διαμοριακές δυνάμεις, πρέπει πρώτα να ξέρουμε για την ηλεκτραρνητικότητα και την πολικότητα του δεσμού.
Ηλεκτραρνητικότητα
Ηλεκτραρνητικότητα είναι η τάση των ατόμων του ομοιοπολικού δεσμού να έλκουν ηλεκτρόνια.
Μία σειρά ηλεκτραρνητικότητας ατόμων που τα συναντούμε συχνά στους ομοιοπολικούς δεσμούς είναι η ακόλουθη:
Όσα από τα στοιχεία διαχωρίζονται με κόμμα, έχουν παρόμοια ηλεκτραρνητικότητα.
Τα στοιχεία C, P και Η έχουν τη μικρότερη ηλεκτραρνητικότητα από τα μη μεταλλικά στοιχεία.
Πόλωση ή πολικότητα ομοιοπολικού δεσμού
Ο ομοιοπολικός δεσμός αναπτύσσεται με δυνάμεις ηλεκτρομαγνητικής φύσης ανάμεσα σε ηλεκτραρνητικά άτομα.
Μη πολικός ομοιοπολικός δεσμός
Όταν οι τιμές ηλεκτραρνητικότητας δύο ατόμων που συνδέονται με ομοιοπολικό δεσμό είναι ίσες, τότε το ζεύγος των ηλεκτρονίων του δεσμού μοιράζεται εξίσου μεταξύ των ατόμων. Ο ομοιοπολικός δεσμός μεταξύ τους λέγεται μη πολικός ομοιοπολικός δεσμός.
Για παράδειγμα το Η2 το Cl2 και το Br2 σχηματίζουν μη πολικούς ομοιοπολικούς δεσμούς.
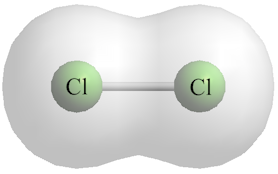
Στους μη πολικούς δεσμούς, το αρνητικό φορτίο των ηλεκτρονίων κατανέμεται ομοιόμορφα στα δύο άτομα.
Εικόνα 1. Η γκρι περιοχή δείχνει την ομοιόμορφη κατανομή του ηλεκτρονιακού νέφους (των ηλεκτρονίων του δεσμού) στα άτομα του Cl. Αυτή η ομοιομορφία στην κατανομή οφείλεται στην ίση ηλεκτραρνητικότητα των δύο ίδιων ατόμων Cl.
Πολικός ομοιοπολικός δεσμός
Όταν ο σχηματισμός του ομοιοπολικού δεσμού γίνεται μεταξύ δύο ατόμων που έχουν διαφορετικές τιμές ηλεκτραρνητικότητας, το πιο ηλεκτραρνητικό άτομο έλκει το ζεύγος των ηλεκτρονίων του δεσμού προς το μέρος του.
Αυτό έχει ως αποτέλεσμα:
- Το κέντρο του θετικού φορτίου του μορίου δε συμπίπτει με το κέντρο του αρνητικού φορτίου του μορίου.
- Λέμε ότι η ηλεκτρονική κατανομή είναι ασύμμετρη μεταξύ των δύο ατόμων.
- Το καθένα από τα δύο άτομα του δεσμού είναι μερικώς φορτισμένο.
- Παριστάνουμε το λιγότερο ηλεκτραρνητικό άτομο του δεσμού με ένα μερικό θετικό φορτίο (που παριστάνεται διεθνώς με δ+) και το πιο ηλεκτραρνητικό άτομο του δεσμού με ένα μερικό αρνητικό φορτίο (που παριστάνεται διεθνώς με δ-).
Λέμε πως ο ομοιοπολικός δεσμός είναι πολικός ή πολωμένος ή ότι συμπεριφέρεται ως ηλεκτρικό δίπολο, όταν σχηματίζεται μεταξύ ατόμων με διαφορετική τιμή ηλεκτραρνητικότητας.
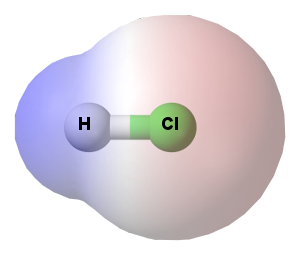
Για παράδειγμα στο μόριο του HCl το Η είναι λιγότερο ηλεκτραρνητικό από το Cl. H κατανομή του αρνητικού φορτίου των ηλεκτρονίων του ομοιοπολικού δεσμού Η-Cl είναι μετατοπισμένη προς τη μεριά του Cl:
Εικόνα 2. Τα δύο άτομα έχουν διαφορετική ηλεκτραρνητικότητα, γι αυτό το μεγαλύτερο μέρος του αρνητικού φορτίου είναι προς τη μεριά του Cl.
Όσο μεγαλύτερη είναι η διαφορά ηλεκτραρνητικότητας μεταξύ των δύο ατόμων που σχηματίζουν τον ομοιοπολικό δεσμό, τόσο πιο πολικός είναι ο δεσμός αυτός (δηλαδή τόσο μεγαλύτερο είναι το μερικό φορτίο δ+ ή δ- που υπάρχει στα άτομα του πολικού ομοιοπολικού δεσμού).
Εικόνα 3. α. Αν το ζεύγος των ηλεκτρονίων ήταν εξίσου μοιρασμένο μεταξύ των δύο ατόμων Η και Cl τότε το μόριο θα ήταν μη πολικό. Αυτό δε συμβαίνει ποτέ μεταξύ διαφορετικών ατόμων που συνδέονται με ομοιοπολικό δεσμό. β. Το ζεύγος των ηλεκτρονίων είναι μετατοπισμένο προς το πιο ηλεκτραρνητικό άτομο (το Cl) με συνέπεια την εμφάνιση κέντρου αρνητικού φορτίου σ’ αυτό (σύμβολο δ–). Η μετατόπιση αυτή δημιουργεί επίσης θετικό φορτίο στο άλλο άκρο του μορίου, που είναι το άτομο του Η (σύμβολο δ+).
Διπολική ροπή μ
Ορισμός διπολικής ροπής μ
Ένα χρήσιμο φυσικό μέγεθος που χρησιμοποιείται για τη μελέτη του κεφαλαίου των διαμοριακών δυνάμεων είναι η διπολική ροπή.
Η διπολική ροπή αποτελεί το μέτρο της πολικότητας (πόλωσης) ενός πολωμένου ομοιοπολικού δεσμού ή ενός μορίου και είναι διανυσματικό μέγεθος. Το μέτρο του δίνεται από τη σχέση : μ = δ r
όπου:
δ: το στοιχειώδες φορτίο (δ+ ή δ-) και
r : η απόσταση των πόλων
Η κατεύθυνση του διανύσματος της διπολικής ροπής δηλώνεται με το σύμβολο: . Το βέλος δείχνει το πιο ηλεκτραρνητικό άτομο του δεσμού.
Το διάνυσμα της διπολικής ροπής μ κατευθύνεται από το θετικό προς το αρνητικό κέντρο ενός πολωμένου ομοιοπολικού δεσμού.
Την έναρξη του διανύσματος τη συμβολίζουμε ένα σταυρό + που δηλώνει το κέντρο θετικού μερικού φορτίου του δεσμού.
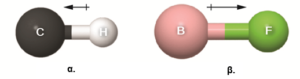
Εικόνα 4. (α) Υπάρχει μικρή διαφορά στην τιμή της ηλεκτραρνητικότητας του C και του Η, η τιμή της διπολικής ροπής μ του δεσμού είναι μικρή και παριστάνεται με ένα μικρό διάνυσμα διπολικής ροπής. (β) Η διαφορά ηλεκτραρνητικότητας ανάμεσα στο Β και το F είναι μεγαλύτερη, οπότε το μήκος του διανύσματος της διπολικής ροπής είναι μεγαλύτερο.
Παράγοντες από τους οποίους εξαρτάται η διπολική ροπή μ
Η διπολική ροπή μ ενός δίπολου μορίου εξαρτάται από την πόλωση των δεσμών (όσο μεγαλύτερη είναι η διαφορά ηλεκτραρνητικότητας ανάμεσα στα άτομα του δεσμού τόσο μεγαλύτερη είναι η διπολική ροπή του δεσμού).
Στα μόρια που περιέχουν περισσότερα από δύο άτομα, στην τιμή της διπολικής ροπής παίζει ρόλο η γεωμετρία του μορίου.
Αυτό είναι λογικό γιατί η τιμή της διπολικής ροπής μ του μορίου, υπολογίζεται από το διανυσματικό άθροισμα των διπολικών ροπών των δεσμών που περιέχονται στο μόριο της ένωσης.
Μη πολικά μόρια
Τα μόρια των ομοιοπολικών ενώσεων με μηδενική διπολική ροπή (μ=0), λέγονται μη πολικά μόρια.
Όλα τα μόρια των στοιχείων που περιέχουν ομοιοπολικούς δεσμούς έχουν μηδενική διπολική ροπή, δηλαδή είναι μη πολικά μόρια. Αυτό είναι αναμενόμενο αφού αποτελούνται από όμοια άτομα, οπότε οι δεσμοί τους είναι μη πολικοί.
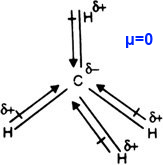
Υπάρχουν μόρια, όπως του CH4, που ενώ έχουν πολωμένους δεσμούς συνολικά δεν εμφανίζουν διπολική ροπή, λόγω συμμετρίας του μορίου.
Εικόνα 5. Στο CH4 η συνολική διπολική ροπή του μορίου είναι μηδέν, γιατί το διανυσματικό άθροισμα των τεσσάρων διανυσμάτων είναι μηδενικό εξαιτίας του σχήματος του μορίου στο χώρο.
Πολικά μόρια (ή δίπολα μόρια)
Όσα μόρια έχουν μη μηδενική διπολική ροπή λέγονται πολικά μόρια ή δίπολα μόρια.
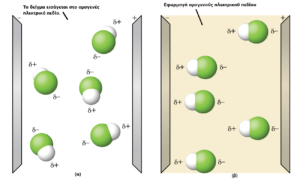
Τα πολικά ομοιοπολικά μόρια συμπεριφέρονται ως ηλεκτρικά δίπολα, αν και το συνολικό τους φορτίο είναι μηδενικό. Αυτό σημαίνει ότι αν τοποθετηθούν εντός ομογενούς ηλεκτρικού πεδίου προσανατολίζονται όλα με τον ίδιο τρόπο, τo αρνητικό άκρο του μορίου προς τη θετική πλευρά του πεδίου και το θετικό άκρο του μορίου προς την αρνητική πλευρά του πεδίου.
Εικόνα 6. (α) Τα μόρια μόλις έχουν εισαχθεί στο ομογενές ηλεκτρικό πεδίο, δεν έχουν αλληλεπιδράσει με το πεδίο και γι αυτό δεν είναι προσανατολισμένα. (β) Τα μόρια μόλις έχουν αλληλεπιδράσει με το πεδίο και γι αυτό είναι προσανατολισμένα.
Πολικά μόρια δύο διαφορετικών ατόμων
Είναι προφανές, πως οι όλες οι ομοιοπολικές ενώσεις που το μόριό τους αποτελείται από δύο διαφορετικά άτομα, έχουν μη μηδενική (μ≠0) διπολική ροπή και είναι πολικά μόρια. Παράδειγμα τέτοιου μορίου είναι το HCl.
Για παράδειγμα στον πολωμένο ομοιοπολικό δεσμό του ΗCl είναι:
Εικόνα 7. Η διπολική ροπή που αντιστοιχεί στον πολικό δεσμό Η-Cl του HCl
Πολικά μόρια με περισσότερα από δύο άτομα
Το τριχλωρομεθάνιο CHCl3 είναι ένα πολικό μόριο. Οι τρεις δεσμούς C – Cl είναι πολικοί με ίσα μέτρα διπολικής ροπής μ.
Η διπολική ροπή του δεσμού C – H είναι σχεδόν μηδενική, γιατί οι ηλεκτραρνητικότητες των δύο αυτών ατόμων είναι περίπου ίσες (η ηλεκτραρνητικότητα του C είναι 2,5 είναι και του Η είναι 2,1). Έτσι η άθροιση των τεσσάρων αυτών διπολικών ροπών δίνει μια συνολική διπολική ροπή η οποία είναι μη μηδενική και αντιστοιχεί στη διπολική ροπή του μορίου.
Το διάνυσμα της διπολικής ροπής του CHCl3 είναι κατακόρυφο με κατεύθυνση προς το χλώριο. Η ύπαρξη διπολικής ροπής δηλώνει την ασύμμετρη ηλεκτρονική κατανομή στο μόριο.
Εγκυκλοπαιδικές γνώσεις
Η ηλεκτρονική κατανομή στα μόρια και στα ιόντα προσδιορίζεται με μία μέθοδο που ονομάζεται φασματοσκοπία ακτίνων-Χ.
Τα μόρια ακτινοβολούνται με ακτίνες Χ γνωστής ενέργειας και μετρούμε την ενέργεια που εκπέμπουν τα ηλεκτρόνια της ουσίας. Έτσι βρέθηκε πως στο θειικό ανιόν (SO42-), το S έχει ένα φορτίο που αντιστοιχεί σε 1,12 μονάδες φορτίου ενώ το κάθε Ο έχει φορτίο που αντιστοιχεί σε -0,78 μονάδες.
Δυνάμεις διπόλου – διπόλου
Ορισμός δυνάμεων διπόλου – διπόλου
Στα πολικά μόρια οι διαμοριακές ελκτικές δυνάμεις είναι ηλεκτροστατικής φύσης μεταξύ των ετερώνυμα φορτισμένων άκρων, πόλων, των μορίων και λέγονται δυνάμεις διπόλου – διπόλου.
Η ισχύς των δυνάμεων διπόλου – διπόλου
Η ισχύς των δεσμών αυτών αυξάνει όσο αυξάνει η διπολική ροπή των μορίων (με την προϋπόθεση τα μόρια να έχουν περίπου την ίδια μάζα και όγκο).
Συνέπειες στο σημείο πήξης και βρασμού των δυνάμεων διπόλου – διπόλου
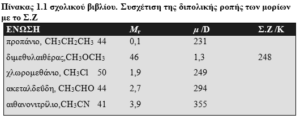
Όσο ισχυρότερες είναι οι δυνάμεις διπόλου – διπόλου, τόσο «ευκολότερα» υγροποιείται ένα αέριο σώμα, δηλαδή τόσο μεγαλύτερο σημείο βρασμού έχει. Και ανάποδα, όσο μικρότερες είναι οι διαμοριακές δυνάμεις, τόσο «δύσκολα» υγροποιείται ένα αέριο. Αυτό φαίνεται και στον παρακάτω πίνακα:
Στον πίνακα φαίνονται πως μόρια με παρόμοιο Mr εμφανίζουν διαφορετική διπολική ροπή. Όσο μεγαλύτερη είναι η διπολική ροπή του μορίου, τόσο μεγαλύτερο είναι και το σημείο ζέσης του (η σταθερή θερμοκρασία στην οποία το υγρό γίνεται αέριο σε καθορισμένη πίεση). Μόρια με υψηλότερα σημεία ζέσης κατέχουν την υγρή κατάσταση ενώ μόρια με μικρά σημεία ζέσης κατέχουν την αέρια κατάσταση.
Όταν δύο πολικά μόρια π.χ. μόρια HCl βρεθούν με κατάλληλο προσανατολισμό, όπως φαίνεται στο παρακάτω σχήμα, έλκονται μεταξύ τους και πλησιάζουν το ένα στο άλλο (το δ+ του ενός μορίου με το δ- του γειτονικού δίπολου μορίου). Με αυτό τον τρόπο αποκτούν μικρότερη ενέργεια και μεγαλύτερη σταθερότητα.
Εικόνα 9. Προσανατολισμένα δίπολα μόρια του HCl. Μεταξύ τους ασκούνται ελκτικές δυνάμεις διπόλου – διπόλου. Τα μόρια αποκτούν ελάχιστη ενέργεια και μέγιστη σταθερότητα.
Μεταξύ των μορίων διπόλου – διπόλου που δεν είναι προσανατολισμένα ασκούνται και ελκτικές και απωστικές δυνάμεις.
Εγκυκλοπαιδικές γνώσεις
Οι ελκτικές δυνάμεις ασκούνται για περισσότερη ώρα από τις απωστικές και υπερισχύουν.
Δυνάμεις διασποράς (London)
Είναι γνωστό ότι και τα μη πολικά μόρια των στοιχείων, όπως π.χ. του Ηe, H2, O2, N2, μπορούν σε πολύ χαμηλές θερμοκρασίες (κοντά στο απόλυτο μηδέν) να συμπυκνωθούν σε υγρά (το φαινόμενο λέγεται υγροποίηση μη πολικών αερίων). Άρα μεταξύ των μη πολικών μορίων θα πρέπει επίσης να ασκούνται κάποιες ελκτικές δυνάμεις.
Το 1926 ο Γερμανός Fritz London (1900-1954) πρότεινε μία εξήγηση για τις δυνάμεις αυτές.
Ας πάρουμε για παράδειγμα τα άτομα He.
Η μέση κατανομή των ηλεκτρονίων γύρω από κάθε πυρήνα είναι συμμετρική (σφαιρική). Τα άτομα είναι μη πολωμένα και δεν παρουσιάζουν διπολική ροπή.
Η στιγμιαία κατανομή των ηλεκτρονίων δεν παρουσιάζει συνεχώς την ίδια εικόνα, όπως φαίνεται στο σχήμα 10α. Σε κάποιο κλάσμα του χρόνου και τα δύο ηλεκτρόνια του ατόμου του He είναι προς το ένα άκρο του φορτίζοντάς το, στιγμιαία, αρνητικά. Τότε, το άλλο άκρο φορτίζεται θετικά και έτσι, δημιουργούνται στιγμιαία δίπολα. Μεταξύ των στιγμιαίων αυτών διπόλων αναπτύσσονται ασθενείς ελκτικές δυνάμεις, οι οποίες ονομάζονται δυνάμεις London ή διασποράς (επειδή οι δυνάμεις δεν έχουν μια ορισμένη κατεύθυνση).
Εικόνα 10. α. Συμμετρική μέση κατανομή ηλεκτρονίων σε δύο άτομα He. Το κάθε άτομο ηλίου έχει σφαιρική κατανομή ηλεκτρονίων. β. Σχηματισμός στιγμιαίων δίπολων και έλξη μεταξύ τους με δυνάμεις London (ή αλλιώς διασποράς).
Η ισχύς των δυνάμεων London (ή διασποράς)
Η ισχύς των δυνάμεων London (ή διασποράς) εξαρτάται από δύο σημαντικούς παράγοντες:
1. Από τη σχετική μοριακή μάζα, Mr. Στα μεγάλα μόρια η κατανομή των ηλεκτρονίων διαταράσσεται ευκολότερα, με αποτέλεσμα να δημιουργούνται στιγμιαία δίπολα. Δηλαδή, η ισχύς των διαμοριακών δεσμών μεγαλώνει με την αύξηση της σχετικής μοριακής μάζας.
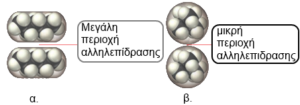
2. Από το σχήμα των μορίων. Γενικώς τα ευθύγραμμα μη πολωμένα μόρια εμφανίζουν ισχυρότερους δεσμούς από τα σφαιρικά μη πολωμένα (διακλαδισμένα), γιατί στα γραμμικά μόρια γίνεται καλύτερη επαφή – αλληλοεπίδραση μεταξύ των μορίων.
Ως παράδειγμα φέρνουμε το κανονικό πεντάνιο, που έχει Σ.Ζ. περίπου 5 °C μεγαλύτερο από το αντίστοιχο του 2,2-διμεθυλοπροπανίου.
Εικόνα 11 α. Το πεντάνιο έχει μεγαλύτερη επιφάνεια, άρα δημιουργεί περισσότερα σημεία επαφής με τα γειτονικά του μόρια και έτσι δημιουργεί ισχυρότερους δεσμούς London. β. Το 2,2 – διμεθυλοπροπάνιο έχει σφαιρική επιφάνεια, μικρότερη από το ισομερές του πεντάνιο, άρα έχει λιγότερα σημεία επαφής με τα γειτονικά του μόρια και συνεπώς ασθενέστερους δεσμούς London.
Οι δεσμοί διασποράς (London) εμφανίζονται σε όλα τα μόρια ανεξάρτητα αν είναι πολωμένα ή όχι.
Δυνάμεις Van der Waals
Ο Van der Waals, το 1873, για να εξηγήσει τις αποκλίσεις των πραγματικών αερίων από την καταστατική εξίσωση των ιδανικών ή τελείων αερίων, ανέφερε την ύπαρξη διαμοριακών δυνάμεων και γι αυτό αναφέρονται γενικώς ως δυνάμεις Van der Waals, οι διαμοριακές δυνάμεις μεταξύ μορίων:
- διπόλου – διπόλου,
- διπόλου – μη διπόλου και
- μη διπόλων
Δεσμοί ιόντος – διπόλου
Στην κατηγορία των ενδομοριακών δεσμών μερικές φορές περιλαμβάνονται και δεσμοί μεταξύ μορίων και ιόντων.
Η ισχύς των δεσμών αυτών εξαρτάται από:
- το μέγεθος και το φορτίο των ιόντων,
- το μέγεθος και τη διπολική ροπή του μορίου.
Στην περίπτωση αυτή το θετικό και αρνητικό ιόν έλκει αντίστοιχα το αρνητικό μέρος και θετικό μέρος του μορίου, όπως φαίνεται στο σχήμα.